BionTec – Modern – Astra Zeneca – Sputnic V
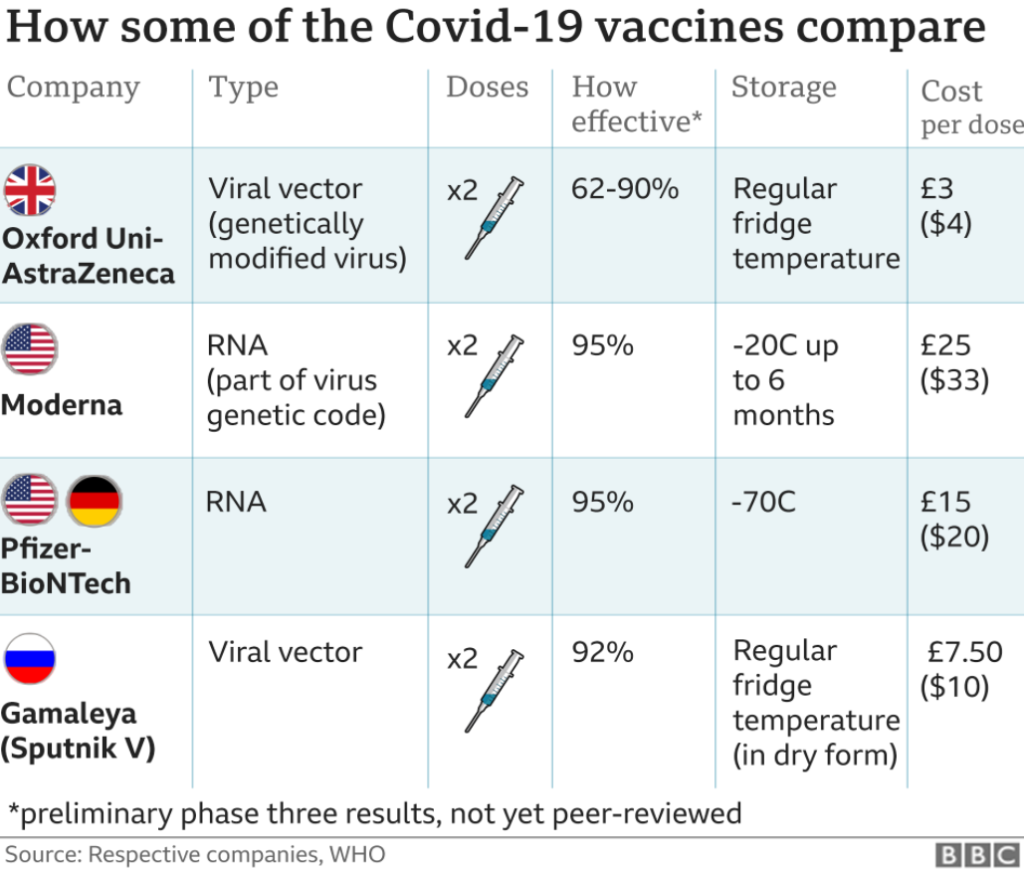
Die vielversprechendsten Covid-19-Impfstoffe
BioNTech, Fosun Pharma und Pfizer
mRNA Impfstoff
95% Schutz
BioNTech, mit Sitz in Mainz, hat sich mit den Pharmafirmen Pfizer und Fosun Pharma zusammengetan.
- Am 18. November 2020 verkündeten die Unternehmen, dass die entscheidenden klinischen Tests an BNT162b2, die vor einer Zulassung nötig sind, abgeschlossen seien.
- Wie sich bereits in einer Zwischenanalyse angedeutet hatte, zeigt der Impfstoff eine hohe Wirksamkeit. Zudem habe er sich bisher als sicher erwiesen.
- BNT162b2 ist mittlerweile unter dem Handelsnamen Comirnaty bekannt.
- Nach aktuellem Kenntnisstand schützt das Vakzin etwa 95 von 100 geimpften Menschen vor einer Covid-19-Erkrankung.
- Der Schutz tritt meist nach der zweiten Impfdosis ein, die im Abstand von drei Wochen nach der ersten Impfung verabreicht werden soll.
- Wie lange der Schutz anhält ist nicht bekannt.
- Auch kann erst während der Impfkampagne ermittelt werden, ob und wie gut Comirnaty auch die Übertragung des Virus bremsen kann.
- Aktuell ist der Impfstoff in mehr als 40 Ländern vorübergehend, bedingt oder per Notfallverordnung zugelassen.
- Für alle 27 EU-Staaten erteilte die EU-Kommission nach Empfehlung der Europäischen Arzneimittelbehörde Ema am 21. Dezember 2020 die bedingte Marktzulassung.
- Zuvor schon hatte die Ema erste Schritte für die Zulassung von Comirnaty unternommen. In einem sogenannten Rolling-Review-Verfahren wurden die bisher verfügbaren Daten zum Impfstoff geprüft, während die finalen Ergebnisse der Studien später eingereicht werden.
- Am 18. November 2020 verkündeten die Unternehmen, dass die entscheidenden klinischen Tests an BNT162b2, die vor einer Zulassung nötig sind, abgeschlossen seien.
- Wie sich bereits in einer Zwischenanalyse angedeutet hatte, zeigt der Impfstoff eine hohe Wirksamkeit.
- Nach aktuellem Kenntnisstand schützt das Vakzin etwa 95 von 100 geimpften Menschen vor einer Covid-19-Erkrankung.
- Dieser Schutz tritt meist nach der zweiten Impfdosis ein, die im Abstand von drei Wochen nach der ersten Impfung verabreicht werden soll. Wie lange der Schutz anhält ist nicht bekannt. Auch kann erst während der Impfkampagne ermittelt werden, ob und wie gut Comirnaty auch die Übertragung des Virus bremsen kann.Aktuell ist der Impfstoff in mehr als 40 Ländern vorübergehend, bedingt oder per Notfallverordnung zugelassen. Für alle 27 EU-Staaten erteilte die EU-Kommission nach Empfehlung der Europäischen Arzneimittelbehörde Ema am 21. Dezember 2020 die bedingte Marktzulassung. Zuvor schon hatte die Ema erste Schritte für die Zulassung von Comirnaty unternommen. In einem sogenannten Rolling-Review-Verfahren wurden die bisher verfügbaren Daten zum Impfstoff geprüft, während die finalen Ergebnisse der Studien später eingereicht werden.
Moderna und NIAID
mRNA Impfstoff
94% Schutz
- Das US-amerikanische Biotechnologieunternehmen Moderna das erste, das seinen Impfstoffkandidaten an Menschen getestet hat.
- Seine Studien führt das Unternehmen gemeinsam mit dem National Institute of Allergy and Infectious Diseases (NIAID) durch, einem Forschungsinstitut der US-amerikanischen Gesundheitsbehörde.
- Der Impfstoff mRNA-1273 ist ein Erbgut-basierter Impfstoff.
- Ein Bericht über die erste klinische Studie wurde im Fachmagazin NEJM veröffentlicht (Jackson et al., 2020). Inzwischen hat die US-Firma Studienergebnisse gemeldet mit einer über 94-prozentigen Impfstoffwirksamkeit.
- Seit dem 18. Dezember ist das Vakzin per Notfallzulassung in den USA auf dem Markt, Kanada erteilte eine vorübergehende Zulassung am 23. Dezember.
- Für die EU will die Europäische Arzneimittelbehörde Ema am 6. Januar 2021 über eine Zulassung entscheiden.
University of Oxford und AstraZeneca
Vektor-Impfstoff
70% Schutz
- Vektor-Impfstoff×Forschende der britischen University of Oxford haben ihren Impfstoff gemeinsam mit dem Pharmakonzern AstraZeneca entwickelt.
- Die Impfung namens AZD1222, in Studien als ChAdOx1-S bekannt, funktioniert nach dem Prinzip eines Vektor-Impfstoffs. Als Vehikel dient in diesem Fall ein Adenovirus, das häufig als Vektor genutzt wird und dafür bekannt ist, beim Menschen unter anderem erkältungsähnliche Symptome auszulösen.
- Ein Bericht zur erfolgreichen Testung in den Phasen I und II erschien im Fachmagazin The Lancet (Folegatti et al., 2020).
- Das Vakzin soll im Mittel einen 70-prozentigen Schutz vor einer Covid-19-Erkrankung bieten.
- Bei spezieller Dosierung könnte die Wirksamkeit womöglich höher liegen.
- Am 30. Dezember erhielt der Impfstoff in Großbritannien erstmals weltweit eine Zulassung. Mit der Auslieferung soll am 4. Januar 2021 begonnen werden, kündigte der britische Gesundheitsminister Matt Hancock an.
- Die Europäische Arzneimittelbehörde Ema hat ebenfalls Schritte für die Zulassung von ChAdOx1-S unternommen. In einem sogenannten Rolling-Review-Verfahren werden die bereits verfügbaren Daten zum Impfstoff bereits geprüft.
- Erweist sich der Impfstoff jedoch nicht als wirksam oder sicher genug, kann das Verfahren abgebrochen werden.
- Am 9. September 2020 gab AstraZeneca bekannt, dass die Tests mit ChAdOx1-S vorübergehend ausgesetzt wurden.
- Man müsse den Fall eines Patienten untersuchen, bei dem eine möglicherweise gravierende Nebenwirkung aufgetreten sei. Nun werde geprüft, ob die gesundheitlichen Probleme vom Impfstoff ausgelöst wurden.
- Dieses Vorgehen ist Standard in der Impfstoffentwicklung. Während so einer Unterbrechung werden keine weiteren Studienteilnehmer geimpft und bisher geimpfte Personen weiterhin beobachtet. Phase-III-Studien sind unter anderem dafür gedacht, mögliche seltene Nebenwirkungen zu entdecken. Einige Tage später wurde die Studie fortgesetzt.
CureVac
mRNA
- in Phase III und II
- Erbgut-basierter Impfstoff×Am 3. Dezember 2020 meldete CureVac als weiteres deutsches Unternehmen die finalen klinischen Studien vor der Zulassung für seinen Impfstoff an.
- CVnCoV enthält wie die Kandidaten von Moderna und BioNTech mRNA-Schnipsel, mit denen der Körper seine Impfung selbst herstellt.
- CureVac hat die Studien der Phasen II und III zusammengelegt und plant, 36.500 Probandinnen und Probanden dafür zu rekrutieren.
Institute of Medical Biology
Impfstoff mit ganzem Virus
- in Phase III×
- Mit inaktivierten Viren möchte das chinesische Institut of Medical Biology seine Impflinge gegen Covid-19 schützen.
- Das Institut in der südchinesischen Stadt Kunming gehört zur Chinese Academy of Medical Sciences.
- An der Phase-III-Stude, die Anfang Dezember 2020 gestartet wurde, sollen mehr als 30.000 Menschen teilnehmen.
Osaka University,
AnGes und Takara Bio
mRNA
in Phase III×
- in Phase II×
- Erbgut-basierter Impfstoff×Aus Japan, entwickelt von Forschenden der Universität Osaka, kommt ein weiterer Erbgut-basierter Impfstoff.
- Wie der Impfstoff der US-Firma Inovio Pharmaceuticals enthält er DNA-Schnipsel, die als Vorlage dienen, damit der Körper die Impfung selbst herstellt.
- Die Vakzine namens AG0302-COVID19 wird seit Anfang Dezember 2020 in den Phasen II und III gleichzeitig getestet – zunächst nur an 500 Probandinnen und Probanden. Später sollen die Tests, wenn möglich, ausgeweitet werden.
Medicago
Virus-ähnlicher Impfstoff
- Medicago
- in Phase III×
- in Phase II×
- Mit Medicago mit Sitz in Québec ist auch ein kanadisches Unternehmen eines der weitesten mit seinen Impfstofftests.
- Sein Kandidat CoVLP funktioniert nach einem anderen Prinzip als herkömmliche Impfstoffe.
- Er enthält sogenannte virusähnliche Partikel (VLPs), die die Struktur des Coronavirus nachahmen.
- Medicago stellt diese VLPs in Pflanzenzellen her. Üblicherweise werden solche Proteine in Zellen von Tieren hergestellt.
- Getestet wird der Impfstoff dem Studienregister zufolge an etwas mehr als 30.000 Menschen.
Inovio Pharmaceuticals und International Vaccine Institute
DNA
- in Phase III×
- in Phase II×
- Das US-amerikanische Unternehmen Inovio Pharmaceuticals ist das erste, das einen Kandidaten in die späten Studienphasen bringt, der auf DNA basiert.
- Zuvor hatten es nur mRNA-Impfstoffe so weit geschafft.
- INO-4800 soll in den USA getestet werden. Die Studien der Phase II und III wurden dafür zusammengelegt.
- Inovio Pharmaceuticals arbeitet an dem Kandidaten gemeinsam mit der NGO International Vaccine Institute, die auf Initiative der UN die Entwicklung von Impfstoffen unterstützt.
Anhui Zhifei Longcom Biopharmaceutical
Virus-Proteine
- in Phase III×
- Als fünftes Team aus China hat eine Arbeitsgruppe des Unternehmens Anhui Zhifei Longcom Biopharmaceutical Ende November 2020 eine Studie der Phase III für seinen Impfstoffkandidaten angemeldet.
- Die Impfung namens ZF2001 enthält ausgewählte Virus-Proteine und einen Wirkverstärker (Adjuvans).
- Getestet wird die Vakzine dem chinesischen Studienregister zufolge an knapp 30.000 Menschen in China.
- Das Projekt betreut das Unternehmen gemeinsam mit dem Institute of Microbiology von der chinesischen Akademie der Wissenschaften.
Bharat Biotech
ganzes, inaktiviertes Virus
- in Phase III×
- Im November meldete ein indisches Unternehmen die vor der Zulassung finale klinische Untersuchung für seinen Impfstoff namens Covaxin oder BBV152 an.
- Bharat Biotech hat seinen Sitz in der zentral-indischen Stadt Hyderabad und möchte seinen zunächst knapp 26.000 Impflingen ein ganzes, inaktiviertes Virus verabreichen.
- Entwickelt wurde der Kandidat in Zusammenarbeit mit dem Indian Council of Medical Research (ICMR) und dem Nationalen Institut für Virologie (NIV).
Novavax
Virus-Proteine
in Phase III×
- Nach erfolgsversprechenden Voruntersuchungen kündigte Ende September 2020 auch das US-amerikanische Unternehmen Novavax an, seinen Impfstoffkandidaten NVX-CoV2373 in den finalen Phase-III-Studien testen zu können.
- Die Vakzine enthält dem Hersteller zufolge ausgewählte Antigene, also Proteine von dem für das Coronavirus charakteristische Spike-Protein, an dem das Immunsystem ansetzt, um das Virus zu bekämpfen.
- Dazu soll ein chemischer Wirkverstärker, genannt Adjuvans, verabreicht werden.
- NVX-CoV2373 wird zunächst an rund 10.000 Probandinnen und Probanden aus Großbritannien getestet.
- Die Hälfte davon bekommt ein Placebo. In den Phasen I und II hatte der Impfstoff gezeigt, dass er eine Immunantwort auslösen kann und auch sicher sein könnte (NEJM: Keech et al., 2020). Ob er tatsächlich vor Covid-19 schützt und keine schwerwiegenden Nebenwirkungen hat, muss er nun beweisen.
Sinovac
ganzer Virus
in Phase III×
- Der chinesische Pharmakonzern Sinovac ist einen bereits gut erprobten Weg gegangen und will Impflingen einen Totimpfstoff verabreichen.
- Bei Untersuchungen an Rhesusaffen zeigte der Impfstoffkandidat CoronaVac bereits Erfolge (Science: Gao et al., 2020).
- In Brasilien und in Indonesien laufen derzeit zwei Studien an mehreren Tausend Freiwilligen.
- Anfang November verkündete das Butantan Institute, das die Studien in Brasilien durchführt, einen vorübergehenden Stopp des Verfahrens.
- Es habe einen “schwerwiegenden Zwischenfall” gegeben, der nun untersucht werden müsse. Klinische Studien werden routinemäßig unterbrochen, wenn es einen Krankheitsfall unter Probandinnen und Probanden gibt.
- Mittlerweile läuft die Studie weiter.
Sinopharm und Wuhan Institute of Biological Products I.
ganzer Virus
- in Phase III×
- Das chinesische Pharmaunternehmen Sinopharm hat zwei Impfstoffkandidaten im Rennen.
- Bei beiden handelt es sich um Totimpfstoffe.
- Einer davon wird von einer Forschergruppe am Wuhan Institute of Biological Products entwickelt.
Sinopharm und Beijing Institute of Biological Products II.
ganzer Virus
86% Schutz
in Phase III×
- Der zweite Kandidat des chinesischen Pharmaunternehmens Sinopharm stammt von Forschenden am Beijing Institute of Biological Products.
- Für beide Kandidaten wurden die Studien in den Vereinigten Arabischen Emiraten (VAE) angesetzt.
- Anfang Dezember kündigte das Gesundheitsministerium der VAE an, für den Impfstoff des Beijing Institute of Biological Products eine Zulassung zu erteilen.
- Eine Zwischenanalyse hatte laut einer Mitteilung eine Wirksamkeit von 86 Prozent ergeben.
- Außerdem habe die Impfung in 100 Prozent der Fälle vor einem schweren Verlauf bewahrt. Insgesamt schloss die Phase-III-Studie 31.000 Menschen ein.
- Wie viele davon in der Zwischenanalyse berücksichtigt wurden, gab das Ministerium nicht bekannt.
- Schon im September hatte es eine Notfallzulassung für den Impfstoff erteilt.
Janssen
Vektor-Impfstoff
Zulassung beantragt×
- in Phase III×
- Vektor-Impfstoff×Das belgische Pharmaunternehmen Janssen hat eine Testung seines Impfstoffes Ad26.COV2.S in Phase III ebenfalls offiziell angemeldet.
- Es handelt sich dabei um einen Vektor-Impfstoff mit einem altbewährten Adenovirus als Transportmittel.
- Bei Rhesusaffen wurde der Impfstoff bereits erfolgreich eingesetzt (Nature: Mercado et al., 2020) und
- seit Kurzem ebenso an Menschen in den Testphasen I und II.
- Am 12. Oktober 2020 gab Janssen als zweites Unternehmen bekannt, dass die aktuell laufende Phase-III-Studie vorübergehend unterbrochen wurde.
- Ein Teilnehmer oder eine Teilnehmerin habe zunächst unerklärliche Krankheitssymptome gezeigt, deren Ursprung nun untersucht würde, hieß es in einer Mitteilung.
- Knapp zwei Wochen später vermeldete der Impfstoff-Hersteller die Fortsetzung der Studie.
- Nach einer Überprüfung des Falls und mithilfe der Einschätzung von unabhängigen Experten habe man keine Hinweise dafür gefunden, dass der Krankheitsfall durch die Impfung ausgelöst wurde.
- Anfang Dezember 2020 genehmigte die Europäische Arzneimittelbehörde Ema ein Rolling-Review-Verfahren für Janssens Impfstoff.
Gamaleya-Institut – Sputnik V
Vektor-Impfstoff
angeblich 92% Schutz
in Phase III×
nicht vollständig erprobt×
Die Zulassung eines Impfstoffs Gam-COVID-Vac, auch genannt Sputnik V, vom Moskauer Gamaleya-Institut erregte Anfang August großes Aufsehen.
Der russische Präsident Wladimir Putin hatte verkündet, dass der Impfstoff bald schon in die Großproduktion gehen und zunächst Krankenhauspersonal sowie Lehrerinnen und Lehrern angeboten würde.
Um die 30 Millionen Dosen sollten – so zumindest anfangs angekündigt – bis Ende 2020 produziert werden.
Die Vakzine beruht auf dem gleichen Prinzip wie der Vektor-Impfstoff von Forschenden der Universität Oxford.
Trotz Zulassung hat der Impfstoff die Studien der Phase III noch nicht erfolgreich absolviert.
Diese sind normalerweise eine Grundvoraussetzung dafür, dass überhaupt eine Zulassung für eine Vakzine beantragt werden kann.
Darüber hinaus haben sich seit der russischen Zulassung weitere Schwierigkeiten ergeben, die ein Erreichen der Ziele aus dem August schwierig machen (weitere Informationen dazu finden Sie in diesem Artikel auf ZEIT ONLINE).
CanSino Biologics
Vektor-Impfstoff
- Zulassung×
- in Phase III×
- nicht vollständig erprobt×
- Schon im Juni wurde in China ein Impfstoff gegen Covid-19 zugelassen.
- Die Vektor-Vakzine enthält ein Adenovirus als Vehikel und hat die Studien der Phase III noch nicht durchlaufen – also noch nicht endgültig gezeigt, dass sie sicher und wirkungsvoll ist.
- Ad5-nCoV sei vor allem für den Notfallgebrauch innerhalb des chinesischen Militärs gedacht, berichtete der Hersteller CanSino Biologics auf seiner Website, der den Wirkstoff gemeinsam mit der chinesischen Militärakademie für Wissenschaften entwickelt hat.
- Dass der Impfstoff in den ersten klinischen Studien Erfolge zeigte, berichteten die Forschenden im Mai im Fachmagazin The Lancet (Zhu et al., 2020).
Übersicht zuletzt aktualisiert am 30. Dezember um 9.02 Uhr